虽然造血系统的理想评估应整合众多免疫相关终点(如病理学、免疫表型和功能性免疫毒性测定),但在病理学评估时无法获得研究数据集的情况并不少见,这可能会限制仅根据病理学结果明确确定毒性作用或确定不良反应的能力。在缺乏功能性或其他免疫学数据的情况下,然后让病理学家确定病理结果是否是不利的或是否将不良反应归因于免疫变化。
在单独评估病理数据的情况下,可能需要提供明确且有信心的不良反应判定,因此不良反应判定可在SD的指导下提交给综合毒理学报告。鉴于不良反应评估通常保留在供试品中,我们认为,当没有支持伤害的证据(如功能变化)时,病理不良反应评估可能不合适(或没有必要)。此外,对于非良好实验室规范(Non-GLP)非临床毒性研究(或早期调查研究),病理学不良反应评估通常不适用,因为此类研究通常作为描述性分析,以确定耐受性、确定候选药物选择和/或告知剂量选择,从而可以计划进一步的研究/终点,以便在后续的关键(符合GLP)研究中对目标器官毒性进行识别和合理全面的表征。此外,在可能需要对相同数据进行替代解释的情况下,以后可能会寻求新的迹象。了解供试品的预期药理有助于进行合理的安全性评价。先前的知识可以帮助病理学家和科学家进行适当的研究设计、物种或品系选择(例如,基因工程小鼠、大鼠或小型猪品系的人源化测试系统)、适当的采样时间、组织采集、替代方法、任何增强评估的需要和适当设计、生物标志物监测和/或可能产生免疫系统评估有意义数据的先进方法。
当描述结果时,病理学家传达不利或非不利决定的发病机制和基本原理是很重要的。此外,应避免在病理学子报告中使用限定术语(如“潜在不良”),因为非病理学家受众可能会删除该限定词,以便在后续报告和监管文件中理解“不良”的有效含义。在任何情况下,研究病理学家都应发挥积极作用,为全面评估毒理学概况和确定免疫系统病理结果的不良反应因素发挥积极作用。
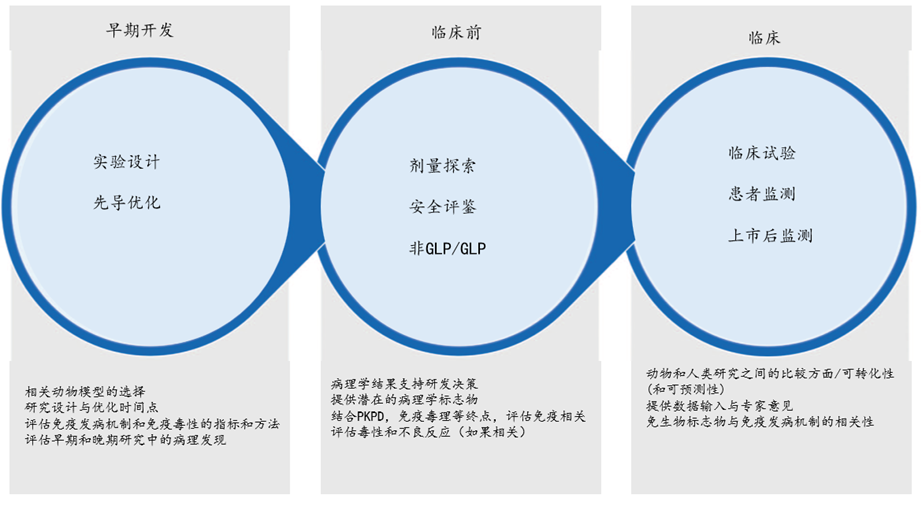
预测成功药物开发的考虑因素
实验动物物种的安全测试、危害识别和挑战模型不能预测临床环境中可能发生的所有不良事件。然而,非临床研究中病理变化的识别和表征以及不良反应评估的基本原理是提醒毒理学家和临床医生注意潜在免疫效应的重要组成部分,无论是否符合预期药理学和/或考虑有毒有害。毒理学家利用病理学报告来确定动物中可能的免疫结果(预期的或非预期的,不利的或非不利的),并对其进行平衡以预测理论上的人类风险。综合来看,非临床物种的研究结果可用于为1期试验中的起始剂量选择、临床监测选项和缓解策略提供信息,并影响支持后期临床试验所需的未来非临床研究计划。重要的是要记住,不良病理结果不一定使有希望的治疗候选药物进入死胡同。例如,在托法替尼(一种免疫抑制性小分子JAK抑制剂)的非临床试验期间,在大鼠和食蟹猴中进行的研究未能确定任何未观察到的不良反应水平(NOAEL),因为在较低剂量组中出现了不良反应。毒性与免疫抑制和免疫器官萎缩有关,从而导致大鼠和猴子严重感染的风险增加,以及猴子淋巴增生效应和血液恶性肿瘤的风险增加。免疫表型和免疫毒理学数据无助于临床监测,并提示对CD4+T辅助细胞的功能性影响。最终,通过产品说明书上的黑框警告处理患者的潜在免疫抑制风险,并通过在特定人群中证实的临床疗效建立有利的风险/效益评估。
跨职能协作
如果非临床研究中的免疫原性、药理学和/或毒理学与人类风险之间的关系仍不确定,病理学家可能会继续就与免疫系统相关的安全性信号进行跨职能对话。虽然非临床研究试图在临床试验中暴露大量患者之前确定安全性问题,但涉及免疫系统的严重不良事件可能要到药物开发的后期阶段才能发现。例如,依法利珠单抗,一种抗CD11a的免疫抑制性人源化单克隆抗体,具有与免疫抑制相关的严重感染风险的最初黑框警告,并最终在患者中由人多瘤病毒2(John Cunningham病毒)引起的4例进行性多灶性脑病(PML)死亡病例后被撤市。因此,重要的是在临床内外持续监测新型免疫疗法的安全性,因为某些药物,例如带有黑框警告的药物或生物制剂,更有可能揭示严重的上市后安全性事件,而这些事件在当前的上市前审查流程中无法评估。具有治疗领域专业知识的病理学家可以继续提供意见,说明如何通过量身定制的研究设计(例如剂量递增、交错招募、临床数据的持续审查)在临床试验中监测和解决不良免疫效应的风险,并明确规定了“停止”标准。
提出了免疫病理学研究结果不良反应决策的实用框架
考虑到不良反应评估的后果,定义什么是不良反应的挑战,以及整个行业对不良反应确定的方法、理念和观点的变化,我们提供了以下关于确定免疫系统不良反应时的考虑因素的意见。理想情况下,在组织评估之前,应向病理学家提供以下信息,以帮助评估、解释和确定不良反应:供试品MOA(包括已知或预计受影响的免疫系统成分)、组和个体免疫相关研究数据(包括免疫表型和免疫功能测试、临床病理学和临床观察)、关于动物和人类反应之间免疫反应变异性(和可转化性)的信息。物种特异性考虑(包括免疫原性和ADA发现,特别是生物制剂),以及预期的患者人群和疾病适应症。
根据非临床研究期间在特定实验条件下对动物造成的“损害”,将不良反应评估给免疫系统结果将适用于不良反应确定的现有******实践。通常,当至少满足以下两个标准时,免疫系统结果的不良反应确定将更有把握:
· 多个免疫器官受到影响(三个或更多初级和/或次级淋巴组织)。
· 对组织和/或关键循环细胞中的显著或较大影响。
· 相关发现(例如,被认为可归因于免疫效应的临床感染或肿瘤,以及功能性免疫毒理学数据)表明对试验物种的危害。
对于免疫系统,在确定不良反应时,最好对所有组织的免疫变化进行综合评估,而不是对单个组织的免疫变化进行综合评估,了解什么构成伤害(以及不良反应)可能需要考虑免疫学、病理学和毒理学因素以及相关数据点。我们认为,免疫结果的不良反应确定应保持灵活性,与环境相关,并结合WOE方法,理想情况下与大量/选定的免疫毒理学相关结果,包括来自单独阶段报告的任何可用的补充数据集。监管机构,以及那些参与药物开发的机构,依靠WOE方法来评估风险,并考虑风险评估策略的许多重要事项。为任何治疗剂开发WOE都是针对该治疗剂的,并且需要在已发表的文献、靶生物学、药代动力学、类别效应、可转化性和临床专业知识的背景下对非临床研究结果进行评估和解释。表4列出了一些病理,免疫毒理学和转化因素通常被纳入制定疾病评估和免疫系统不良反应评估。

总结
目前免疫系统评估的情况与过去几十年有很大不同。由于我们对免疫系统在疾病发病机制中的作用有了更深入的了解,以及我们利用免疫反应预防和治疗疾病的潜力,旨在调节免疫系统的新的、强大的疗法正越来越多地被开发出来,并不仅应用于癌症,还应用于许多其他疾病。正是在这种复杂和快速发展的情况下,病理学家和毒理学家被要求调查疗效和安全性考虑,并决定哪些免疫系统反应在正常变异范围内,哪些反应代表预期(或放大)的药理学,以及何时反应代表毒性表现。因此,科学家个人和组织如何应对为免疫系统结果做出不良反应决策的挑战存在显著差异并不令人惊讶。
在非临床物种中,没有明确的定量和功能性上限和下限阈值,以明确表出免疫系统中几乎所有个体病理结果的不利情况。鉴于免疫系统的广泛分布和动态性质,免疫系统具有巨大的可塑性和储备能力,因此应谨慎对待不良反应的确定,除非有相关的功能证据表明免疫器官的形态变化具有生物学后果。因此,不良反应的确定不能基于一个(甚至几个)参数的公式化方法,而是整体考虑与这些变化相关的可观察的生活后遗症(例如,耐受性和临床症状)。对循环免疫细胞和免疫组织切片中的发现进行全面评估是有利的;因此,应对造血系统的不良反应进行综合评估,并尽可能整合辅助功能数据(即WOE方法)。药物开发方、合同研究组织CRO、政府组织和专业科学协会应致力于免疫系统不良反应测定的协调方法。本文的目的是提供免疫系统评估挑战的简要信息概述,并围绕非临床研究中观察到的免疫系统病理学的合理不良反应确定的当前实践展开论述。
